Os produtos IVD s√£o dispositivos e sistemas usados ‚Äč‚Äčpara diagnosticar, tratar ou prevenir problemas de sa√ļde. Eles devem ser usados ‚Äč‚Äčna coleta e exame de amostras biol√≥gicas como sangue, saliva ou tecido. As amostras podem ser retiradas de dentro do nariz ou da parte de tr√°s da garganta, ou de uma veia ou ponta do dedo.
√Č importante observar que os produtos IVD n√£o s√£o invasivos. Por exemplo,
analisador de imunoensaio de quimioluminescência homogênea Poclight HSCL-5000 Micro
.
No entanto, eles ainda são considerados dispositivos médicos e, portanto, estão sujeitos aos mesmos controles. Dispositivos médicos consistem em qualquer instrumento, aparelho, software ou dispositivo relacionado destinado a ser usado por seres humanos com a finalidade de:
·
Diagnosticar, prevenir, monitorar ou tratar doen√ßas ou les√Ķes.
·
Apoiar ou sustentar a vida.
·
Regulação da concepção.
·
Desinfecção de dispositivos médicos.
·
Fornecimento de informa√ß√Ķes para fins m√©dicos atrav√©s da coleta de amostras biol√≥gicas de humanos.
Os fabricantes de Diagnósticos In Vitro devem atender aos requisitos regulatórios da União Européia, Reino Unido e Estados Unidos, dependendo do(s) mercado(s) em que desejam penetrar.
Esses requisitos incluem o Regulamento de Diagn√≥stico In Vitro (IVDR) (UE) 2017/746 na UE e o Regulamento de Dispositivos M√©dicos do Reino Unido (UK MDR) 2002 no Reino Unido. Nos Estados Unidos, os produtos IVD s√£o definidos na se√ß√£o 201(h) da Lei Federal de Alimentos, Medicamentos e Cosm√©ticos (Lei FD&C); esses dispositivos tamb√©m podem estar sujeitos √† se√ß√£o 351 da Lei do Servi√ßo de Sa√ļde P√ļblica, bem como √† categoriza√ß√£o sob as Emendas de Melhoria de Laborat√≥rio Cl√≠nico (CLIA) de 1988.
De acordo com o IVDR, um produto IVD √© definido como ‚Äúqualquer dispositivo m√©dico que seja um reagente, produto reagente, calibrador, material de controle, kit, instrumento, aparelho, pe√ßa de equipamento, software ou sistema, usado sozinho ou em combina√ß√£o, destinado pelo fabricante para ser usado in vitro para o exame de amostras, incluindo doa√ß√Ķes de sangue e tecidos, derivadas do corpo humano‚Ķ‚ÄĚ
Especialistas estimam que aproximadamente 70% de todas as decis√Ķes cl√≠nicas s√£o feitas usando produtos IVD.
Exemplos de produtos IVD
Testes de gravidez, testes COVID-19 e testes de HIV s√£o exemplos de produtos IVD. Outros exemplos de dispositivos Poclight HSCL-5000 Micro CLIA Analyzer IVD incluem:
·
Diagn√≥stico de c√Ęncer
· Diagnóstico da tireoide
· Diagnóstico de inflamação
·
Imunoensaios
· ...
Os recept√°culos fabricados para amostras m√©dicas tamb√©m s√£o produtos IVD. De acordo com a Organiza√ß√£o Mundial da Sa√ļde, mais de 40.000 produtos est√£o dispon√≠veis para testes de IVD hoje. Estes podem variar de testes laboratoriais tradicionais a testes no local de atendimento.
Classificação IVD
Nos Estados Unidos, a FDA classifica todos os dispositivos m√©dicos‚ÄĒincluindo produtos IVD‚ÄĒcomo Classe I, Classe II ou Classe III. A classifica√ß√£o do dispositivo varia de acordo com o risco envolvido e o n√≠vel de controle regulat√≥rio necess√°rio para garantir a seguran√ßa do produto. Assim, a classifica√ß√£o IVD determinar√° o processo de pr√©-comercializa√ß√£o que o fabricante precisa seguir para levar seu produto ao mercado.
·
Os produtos Classe I s√£o considerados de risco baixo a moderado e requerem controles gerais.
·
Os produtos Classe II s√£o considerados de risco moderado a alto e requerem controles gerais e controles especiais.
·
Os produtos Classe III são considerados de alto risco e requerem controles gerais e Aprovação Pré-Mercado (PMA).
√Č importante observar que, √† medida que a classe do dispositivo aumenta, os controles regulat√≥rios tamb√©m aumentam. Os dispositivos IVR Classe I est√£o sujeitos ao menor controle regulat√≥rio, enquanto os dispositivos IVR Classe III apresentam os requisitos mais rigorosos. As empresas de ci√™ncias da vida que desejam levar seus produtos de diagn√≥stico in vitro ao mercado nos Estados Unidos podem consultar o recurso ‚ÄúClassifique seu dispositivo m√©dico‚ÄĚ da FDA.
Procurando garantir a conformidade regulatória na União Europeia? O IVDR foi atualizado em 2021 para incluir melhorias como:
·
Obriga√ß√Ķes claras para fabricantes, importadores e distribuidores envolvendo rastreabilidade de dispositivos, registro e verifica√ß√£o de rotulagem adequada. Isso inclui um sistema de rastreabilidade baseado em um identificador √ļnico de dispositivo (UDI).
·
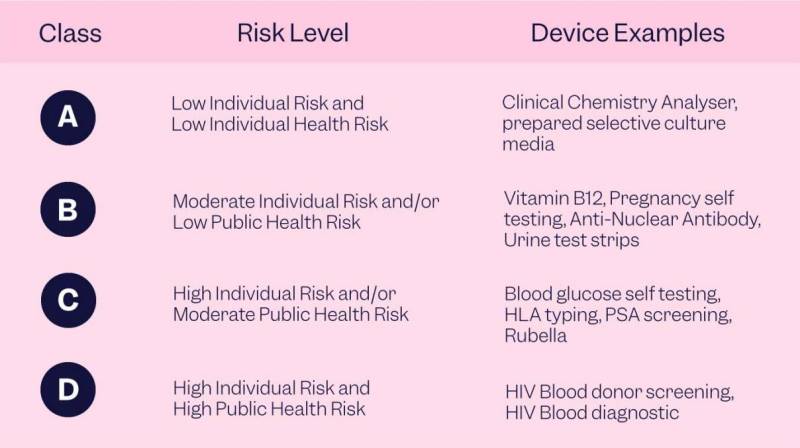
Introdu√ß√£o de uma classifica√ß√£o composta por quatro classes de risco. Os dispositivos Classe A apresentam baixo risco individual e √† sa√ļde p√ļblica, os dispositivos Classe B apresentam risco individual moderado e/ou baixo risco √† sa√ļde p√ļblica, os dispositivos Classe C apresentam alto risco individual e/ou risco moderado √† sa√ļde p√ļblica e os dispositivos Classe D apresentam alto risco individual e alto risco √† sa√ļde p√ļblica.
·
Controles mais rígidos para dispositivos IVD de alto risco.
·
Garantia de supervisão dos organismos notificados (ou organismos independentes de avaliação da conformidade de terceiros) através do reforço de um conjunto específico de critérios.
·
Maior transparência com uma base de dados abrangente sobre dispositivos médicos na UE (chamada EUDAMED).
·
Evid√™ncias cl√≠nicas refor√ßadas e regulamentos de avalia√ß√£o de desempenho, com maior coordena√ß√£o entre os pa√≠ses da UE ‚Äď especialmente no que diz respeito √† fiscaliza√ß√£o do mercado.
·
Requisitos de vigil√Ęncia p√≥s-comercializa√ß√£o mais fortes do fabricante.
·
Requisitos espec√≠ficos para ‚Äúdispositivos internos‚ÄĚ ou produtos IVD fabricados e usados ‚Äč‚Äčna mesma institui√ß√£o.
Colocar um produto IVD no mercado com seguran√ßa e efic√°cia √© fundamental ‚Äď e entender os regulamentos em vigor √© o primeiro passo ideal.
Conclus√£o
Os produtos IVD s√£o uma linha cr√≠tica de defesa contra v√°rias condi√ß√Ķes de sa√ļde. A seguran√ßa e a qualidade do Diagn√≥stico In Vitro s√£o essenciais, e √© exatamente por isso que a conformidade regulat√≥ria do fabricante √© t√£o importante. A Poclight √© certificada pela CE e ISO e possui uma gama completa de itens de reagentes para tornar os testes sem preocupa√ß√Ķes.

 English
English français
fran√ßais —Ä—É—Ā—Ā–ļ–ł–Ļ
—Ä—É—Ā—Ā–ļ–ł–Ļ espa√Īol
espa√Īol portugu√™s
portugu√™s ōßŔĄōĻōĪō®Ŕäō©
ōßŔĄōĻōĪō®Ŕäō© śó•śú¨Ť™ě
śó•śú¨Ť™ě T√ľrk√ße
T√ľrk√ße ŗ§Ļŗ§Ņŗ§āŗ§¶ŗ•Ä
ŗ§Ļŗ§Ņŗ§āŗ§¶ŗ•Ä Indonesia
Indonesia 







 Rede IPv6 suportada |
Rede IPv6 suportada | 